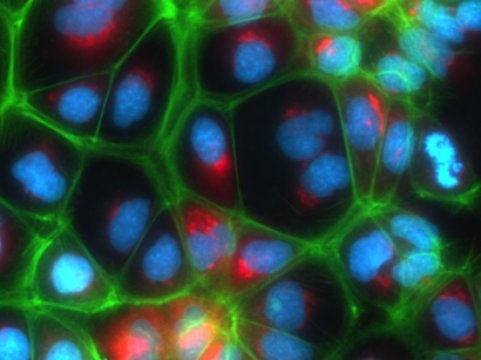
荧光标记的极化Upcyte?肝细胞
供图:Yaakov Nahmias教授
在《自然·生物技术》上发表的一项新研究中,由耶路撒冷希伯来大学领导的一个国际研究团队描述了一种在实验室中培养人类肝细胞的新技术。这一开创性的进步可能会推进一系列肝脏相关的研究和应用,包括从药物毒性研究到为等待肝移植患者提供的人工肝等。
肝脏是人体最大的内脏器官,是主要的新陈代谢场所。人类肝细胞构成肝脏的85%,是制药工业中研究药物毒性、药物清除率及药物间相互作用常用的细胞。肝细胞还应用于临床的细胞疗法、校正遗传缺陷、改善肝硬化,或者支持辅助治疗采用肝脏辅助设备的患者。
遗憾的是,虽然在普罗米修斯的神话中古希腊人已经意识到,人类肝脏可以在活机体内快速再生,然而一旦细胞移至体外,这种增殖能力就会迅速丧失。迄今为止,在实验室条件下尝试的人类肝细胞扩增最后得到的都是无限增殖的低代谢癌细胞。人类肝细胞紧缺,且无法在不丧失其功能的情况下进行扩增,是科研、临床及药物的研究进展的主要瓶颈。
为了解决这一问题,耶路撒冷希伯来大学亚历山大格拉斯生物工程中心主任Yaakov Nahmias与德国upcyte technologies GmbH公司(前Medicyte公司)的首席科学家合作,开发出一种实验室扩大培养人类肝细胞且不丧失其独特代谢功能的技术。
在德国癌症研究中心之前对人乳头瘤病毒(Human Papilloma Virus,HPV)的研究工作的基础上,研究团队证实,低表达的HPV E6和E7蛋白可将肝细胞从细胞周期阻滞中释放出来,并在参与肝细胞再生的白介素6(interleukin 6,IL-6)超家族成员抑癌蛋白M(OSM)的刺激下发生增殖。鉴于在之前的实验中培养的肝细胞发生增殖失控,转变为癌细胞并丧失了代谢功能,科研人员谨慎挑选了只对OSM产生应答发生增殖的人类肝细胞克隆。OSM刺激引起的细胞增殖时间比通常延长了一倍,为33至49小时。移除OSM,肝细胞在4天内会发生生长阻滞、组织分化,从而转变为具有高度功能性的肝细胞。这种方法称为“upcyte? process”(upcyte股份有限公司),可使肝细胞从单个克隆增殖35个倍增群体数,产生1015个克隆。相比之下,从健康器官中只能分离出109个细胞。
“这是个革命性的方法。”德国团队的带头人Joris Braspenning医生说,“这一技术的强大之处在于各类捐赠者的肝细胞均可增殖,使研究患者多样性及肝毒性异质性成为可能。”研究团队从多个种族背景个体取得了可连续传递的肝细胞系,它们同时具有CYP450活性、表皮极性,且与原始人肝细胞蛋白表达水平相同。重要的是,体外培养的肝细胞与原始人肝细胞对23种药物的毒理学反应完全相同。
“这是肝脏研究的圣杯。”该研究的带头人Nahmias教授说,“我们的技术将使全世界上千个实验室研究脂肪肝、各种肝炎、药物毒性及肝癌,而不用如目前花费巨大。”Nahmias指出,基因修饰是细胞用于移植的阻碍,“但我们会为生物人工肝脏项目找到完美的细胞来源”。
增殖的肝细胞库最近由upcyte技术股份有限公司(upcyte technologies GmbH,位于德国汉堡)投入商业运营,该公司目前正在扩大此技术规模。“upcyte?公司的肝细胞代表了下一代细胞技术。”总经理Astrid N?renberg医生说,“我们已经准备好了成为药物研发及化学毒性检测的细胞供应商的领头人。
翻译:谢梦莹
审稿:董子晨曦



















留言